La résistance aux antibiotiques — ou antibiorésistance — est un enjeu de santé publique majeur. Conserver l’efficacité des antibiotiques contre les bactéries passe notamment par comprendre comment ces résistances fonctionnent et comment les bactéries deviennent résistantes. Comme l’explique le CNRS, si aucune action n’est prise, des millions de décès pourraient, chaque année, être imputés à des maladies causées par des bactéries résistantes aux antibiotiques d’ici 2050. Explications à travers les recherches de l’Institut Pasteur et du CNRS.
Les antibiotiques sont des médicaments qui servent à lutter contre les infections dues à des bactéries. Ils ont sauvé et sauvent encore des millions de vies chaque année, mais leur efficacité est menacée car les bactéries peuvent s’adapter et résister au traitement. On parle de résistance aux antibiotiques ou aux antibactériens. « L’antibiorésistance désigne à la fois une dynamique qui existe depuis l’utilisation des antibiotiques, mais aussi l’ensemble des mécanismes que les bactéries utilisent pour résister à ces traitements », résume Didier Mazel responsable de l’unité Plasticité du génome bactérien à l’Institut Pasteur.
Comment les résistances fonctionnent ?
Plusieurs mécanismes de résistance existent et peuvent conduire à une même insensibilité au traitement. La plupart du temps, la bactérie va soit altérer l’antibiotique lui-même, soit la molécule cible avec laquelle celui-ci réagit normalement, ce qui dans les deux cas le rend inefficace. D’autres formes de résistance moins efficaces sont connues, comme la pompe d’efflux, qui permet d’expulser l’antibiotique en dehors de la bactérie.
« La surveillance de l’antibiorésistance passe par la mesure de la fréquence des souches sensibles ou résistantes à un antibiotique, c’est-à-dire la proportion de bactéries devenues insensibles à ce médicament », poursuit Céline Loot, chercheuse dans l’unité de Didier Mazel.
Comment les bactéries deviennent résistantes ?
Quand elles sont confrontées à un antibiotique, les bactéries évoluent : les lignées résistantes se reproduisent mieux et finissent par devenir majoritaires.
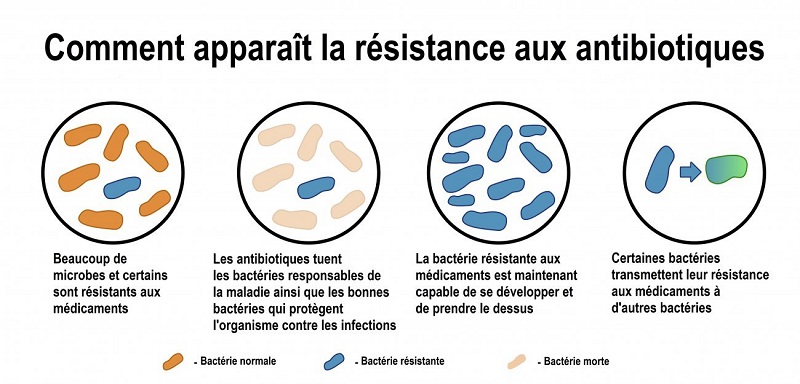
Mais les nouvelles résistances se propagent bien plus vite par des mécanismes dits de « transferts horizontaux » : la résistance se transmet entre des organismes de lignées différentes, et non d’une bactérie à ses descendantes.
- La conjugaison, lorsque des bactéries se transmettent entre elles des petits morceaux de matériel génétique, appelés des plasmides, et qui peuvent porter des gènes qui fournissent des résistances. « Les plasmides peuvent se transmettre entre des genres bactériens très différents, ce qui en fait le mécanisme de transmission de résistances le plus important et celui que nous voudrions le plus contrôler », précise Céline Loot.
- La transformation naturelle, qui a lieu quand une bactérie intègre de l’ADN présent dans son environnement.
- La transduction, qui consiste en un transfert de matériel génétique entre une bactérie et un virus qui l’infecte. Ce mécanisme joue cependant un rôle mineur dans l’acquisition de résistance.
« Tout ce qui va stresser les bactéries va favoriser les transferts horizontaux, alerte Didier Mazel. C’est le cas des antibiotiques même à faible concentration, comme dans les eaux usées où l’on en trouve des traces. C’est d’autant plus le cas là où on concentre des bactéries, comme dans les biofilms, des communautés de cellules qui adhérent aux supports solides, et qui peuvent se former par exemple sur le matériel médical ».
La lutte contre l’antibiorésistance, un enjeu de santé publique
La prévention : Pour combattre l’antibiorésistance, « le plus efficace reste la prévention, souligne Céline Loot. Aujourd’hui, les foyers de la résistance sont en Asie du Sud-Est, où l’on voit une utilisation massive d’antibiotiques sans prescription médicale, qu’il faudrait limiter ».
Des alternatives aux antibiotiques actuels : « Nous sommes en quête de nouvelles molécules dont on aurait une utilisation prudente pour prévenir l’apparition de nouvelles résistances », développe la chercheuse. Les scientifiques développent aussi de nouveaux modes de traitements, « comme les bactériophages, ou rendre de nouveau la bactérie sensible à l’antibiotique. On souhaite aussi empêcher les transferts horizontaux pour limiter la dispersion des résistances. Au final, on devient très créatifs ! », décrit Didier Mazel.
La recherche fondamentale reste nécessaire, puisque c’est sur ces connaissances que s’appuie le développement de nouvelles approches thérapeutiques.
ESKAPEE : sept pathogènes à surveiller
Parmi les bactéries incriminées dans l’antibiorésistance, un groupe de sept pathogènes identifiés sous le terme de bactéries ESKAPEE constitue notamment une menace sérieuse. Ce sont les bactéries résistantes qui représentent le plus un problème de santé publique selon l’OMS, et sur lesquelles la recherche se focalise. Ces bactéries sont à l’origine de nombreuses infections nosocomiales : des infections pulmonaires, urinaires ou post-opératoires, mais aussi parfois des septicémies chez les patients immunodéprimés.
L’antibiorésistance, une menace majeure pour la santé mondiale ?
Christophe Grangeasse, directeur de Recherche CNRS au laboratoire microbiologie moléculaire et biochimie structurale, exprime son inquiétude en rappelant qu’en 2014, une étude britannique alertait déjà sur l’importance « de découvrir de nouvelles molécules capables d’échapper aux processus d’antibiorésistance, sans quoi le nombre de décès liés aux bactéries pourrait atteindre 10 millions de personnes et dépasserait celui des décès dus aux cancers d’ici 2050 ».
Cédric Orelle, directeur de Recherche CNRS dans la même unité, tient à rappeler que « les antibiotiques ont, avant toute chose, révolutionné la médecine moderne. Avant les années 1940, la moindre infection pouvait nous être fatale ! Néanmoins, il relève aussi que, depuis, leur utilisation inappropriée et abusive, y compris dans le contexte des élevages industriels, a généré de graves problèmes ». En effet, des générations de bétail ont été exposées à ces molécules, rendant certaines bactéries de plus en plus résistantes et contraignant les éleveurs à recourir à des doses d’antibiotiques encore plus élevées. En outre, près de la moitié des antibiotiques fabriqués à travers le monde sont destinés à l’élevage et ce chiffre grimpe à 80% aux États-Unis. Une surutilisation qui a entraîné la présence de traces résiduelles d’antibiotiques dans l’environnement : des eaux usées, jusque dans nos assiettes.
Cédric Orelle complète : « Par ailleurs, les rejets de nombreuses autres molécules dans l’environnement (antiseptiques, pesticides, polluants, etc.) ont aussi pu contribuer à la sélection de bactéries résistantes à ces molécules ainsi qu’à certains antibiotiques ». Combinée avec une administration excessive chez l’humain, cette situation a favorisé la prolifération de bactéries résistantes et l’inefficacité d’un nombre croissant de traitements contre certaines infections.
Face à cette menace grandissante, « la recherche scientifique mondiale peine à trouver des molécules avec de nouveaux modes d’action » souligne Christophe Grangeasse. Les avancées les plus récentes en matière de traitements d’infection bactérienne consistent essentiellement en des modifications d’antibiotiques déjà existants. Dès lors, sous l’impulsion de l’Organisation Mondiale de la Santé (OMS) et des agences nationales de recherche, les scientifiques du monde entier se sont récemment remis en ordre de bataille pour trouver de nouvelles stratégies de lutte et prévenir une crise sanitaire mondiale. Un combat qui débute par une étape fondamentale : infiltrer les rangs de l’adversaire pour acquérir une connaissance approfondie de ses mécanismes de fonctionnement.
C’est une approche novatrice, souligne Christophe Grangeasse, qui se souvient qu’au début des années 2000, un dogme scientifique prédominant soutenait que les bactéries – contrairement aux cellules eucaryotes – étaient dépourvues d’un ensemble de protéines régulatrices que l’on appelle des sérine/thréonine protéines kinases (PK) ». Il est maintenant clairement établi que ces PK jouent un rôle central dans la capacité des bactéries à se multiplier et à s’adapter à leur environnement. « Il s’agit d’une avancée fondamentale, insiste le chercheur, car ces protéines pourraient, à terme, être considérées comme de nouvelles cibles thérapeutiques ».
« En utilisant une approche interdisciplinaire alliant l’imagerie cellulaire, la génétique et la biochimie structurale, poursuit-il, nous nous sommes rendu compte que ces PK exerçaient une influence considérable sur l’intégrité de la cellule bactérienne, et donc sur leur survie ».
Les travaux que mènent Christophe Grangeasse et son équipe visent donc à décrypter ces mécanismes de régulation pour, à terme, imaginer des traitements qui puissent directement cibler les PK. Ce nouveau type de médicament affecterait la viabilité de la bactérie et l’empêcherait de s’adapter à son environnement et donc de provoquer une infection.
La bataille est encore longue, mais ces recherches prometteuses menées au laboratoire microbiologie moléculaire et biochimie structurale sont de nature à envisager sereinement l’avenir. Ces travaux très fondamentaux sont cruciaux pour décrire avec précision les mécanismes de régulation qui pourront être la clé de futurs traitements. Une perspective encourageante dans la lutte contre l’antibiorésistance.
Sources :
- Institut Pasteur
- Journal du CNRS (Etude « Résistances aux traitements : la recherche en quête de solutions » réalisé en collaboration avec Pop’Sciences – Université de Lyon (mai 2023).