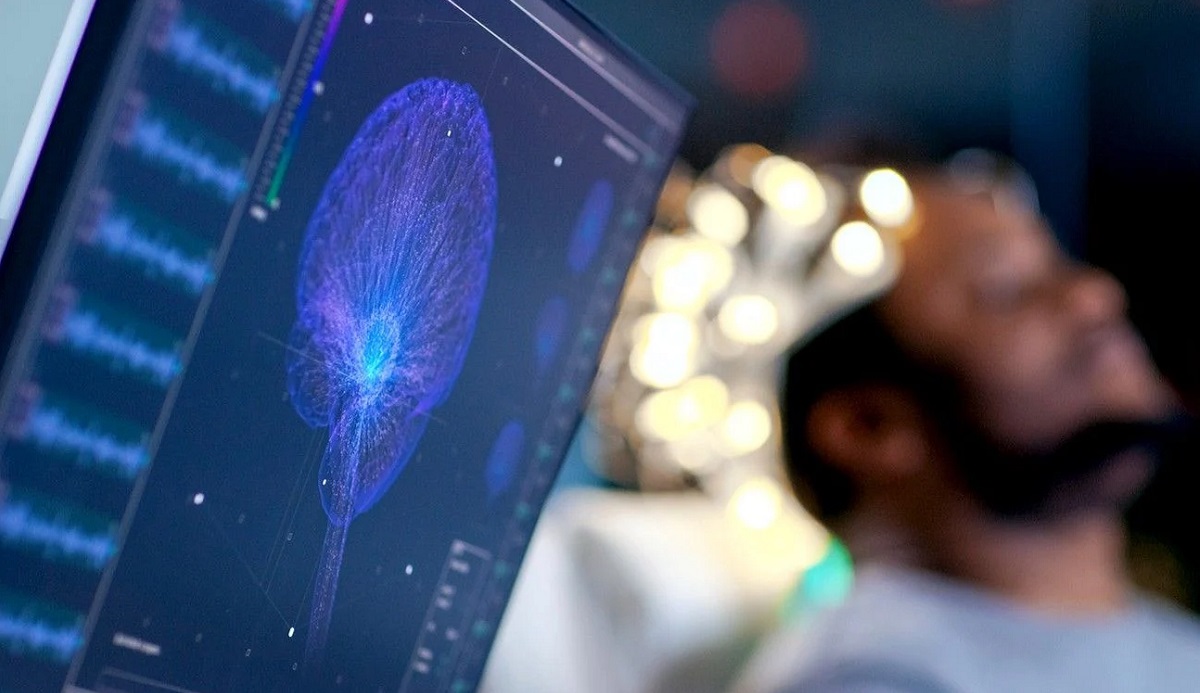
Qu’est-ce qui reste dans un cerveau après un AVC ? Plus qu’on ne le croit. Et c’est précisément là que les interfaces cerveau-machine font leur entrée — non pas pour augmenter l’humain, mais pour le réparer, de l’intérieur. L’interface cerveau-machine est souvent traitée comme une technologie du futur transhumaniste. Or son application la plus concrète et la plus humaniste est d’aider des patients victimes d’AVC à retrouver l’usage de leur corps, en exploitant la plasticité cérébrale. D’autant que les avancées technologiques récentes rendent réels les scénarios de rééducation à domicile. Le cerveau sait encore marcher. Il a juste perdu le fil. Ces interfaces cerveau-machine apprennent aujourd’hui à le renouer — neurone par neurone, intention par intention : une révolution silencieuse qui se passe loin des promesses de Neuralink. Elle se passe dans des chambres de rééducation. Et bientôt, chez vous. Et si le cerveau d’un patient paralysé contenait encore, quelque part, l’intention de bouger ? Et si une machine pouvait l’entendre — et ordonner au corps d’obéir ? Ce n’est plus de la science-fiction. C’est de la neurologie clinique, en 2026.
Les interfaces cerveau-machine peuvent améliorer la récupération motrice après un AVC — c’est désormais un fait scientifique établi, non une promesse technologique. Plusieurs méta-analyses publiées entre 2024 et 2026 dans des revues comme Frontiers in Rehabilitation Sciences et PubMed confirment que les dispositifs BCI (pour Brain-Computer Interface) combinés à des techniques de stimulation permettent aux patients victimes d’accidents vasculaires cérébraux de récupérer des fonctions motrices supérieures à celles obtenues par la rééducation conventionnelle seule. La révolution neurologique est en marche — mais ses contours sont moins spectaculaires, et plus profonds, que ne le laissent entendre les annonces de Neuralink.
Longtemps cantonnées aux laboratoires de neurosciences ou aux promesses transhumanistes de Neuralink, les interfaces cerveau-machine (BCI) font en 2026 une entrée discrète mais décisive dans les services de neurologie. Leur terrain d’application le plus concret — et le plus profondément humain — n’est pas la fusion homme-machine : c’est la salle de rééducation, et bientôt le domicile des victimes d’accidents vasculaires cérébraux.
Le principe est aussi élégant que redoutable : capter en temps réel l’intention motrice d’un patient partiellement paralysé, et la traduire en stimulation électrique ou magnétique des muscles concernés. Ce couplage entre le signal cérébral et la réponse musculaire ne se contente pas de suppléer au déficit neurologique — il le répare, lentement, en forçant le cerveau à reconstruire ses propres circuits endommagés. La neuroplasticité, cette capacité du cerveau à se recâbler après une lésion, cesse d’être une hypothèse de laboratoire : elle devient la cible thérapeutique d’une révolution clinique silencieuse, documentée par plusieurs méta-analyses publiées en 2025 et 2026.
Ce qui change en 2026, c’est l’échelle et l’accessibilité. Des dispositifs portables — comme le Magnetic NeuroRing ou les dispositifs de stimulation magnétique transcrânienne portables de nouvelle génération — rendent désormais envisageable une rééducation à domicile, sans plateau technique hospitalier. Et en France, une nouvelle chercheure, Idoia Quintana-Urzainqui, s’installe en avril 2026 au sein de NeuroPSI (CNRS), portée par le financement de la bourse ERC Consolidator Grant 2025, pour pousser encore plus loin les frontières du possible.
Qu’est-ce qu’une interface cerveau-machine et comment fonctionne-t-elle ?
Une interface cerveau-machine (BCI, Brain-Computer Interface) est un dispositif qui capte les signaux électriques produits par le cerveau — le plus souvent par électroencéphalographie (EEG) — et les traduit en commandes pour un système externe. Dans le contexte de la rééducation post-AVC, ce système externe est un exosquelette ou un stimulateur neuromusculaire : lorsque le patient tente mentalement de bouger un bras paralysé, le BCI détecte l’intention motrice et déclenche une stimulation électrique fonctionnelle des muscles correspondants.
Ce mécanisme exploite un principe fondamental de la neuroplasticité : le fait que le cerveau adulte peut réorganiser ses connexions neuronales en réponse à l’entraînement répété. En associant systématiquement une intention motrice à un mouvement effectif (même induit artificiellement), le BCI renforce les voies neuronales résiduelles et accélère la récupération des circuits moteurs endommagés lors de l’AVC.
Ce que montrent les études cliniques en 2026
Une méta-analyse publiée en 2025 dans Frontiers in Human Neuroscience, portant sur plusieurs revues systématiques, confirme que le traitement par BCI améliore significativement la fonction motrice du membre supérieur chez les patients en phase subaiguë (dans les six premiers mois après l’AVC), avec «un bon profil de sécurité». Les résultats sont plus modestes pour les patients chroniques, mais restent positifs par rapport aux groupes contrôle.
Des avancées technologiques récentes rendent désormais réalisable la rééducation à domicile. Le Magnetic NeuroRing, dispositif portable permettant une stimulation magnétique transcrânienne en temps réel, et d’autres solutions d’électrostimulation fonctionnelle adaptée représentent une rupture : ils permettent d’allonger considérablement la durée et la fréquence des séances de rééducation, sans mobiliser de personnel hospitalier spécialisé.
Les interfaces cerveau-machine peuvent-elles aider à récupérer après un AVC ?
La question n’est plus vraiment de savoir si les interfaces cerveau-machine peuvent aider à récupérer après un AVC — la littérature scientifique y répond désormais par l’affirmative. Elle est de savoir dans quelle mesure, et pour combien de temps.
La méta-analyse de Liu et al., publiée en mars 2025 dans Frontiers in Human Neuroscience, établit clairement que les BCI offrent des avantages mesurables sur les programmes de rééducation traditionnels : meilleure récupération motrice, neuroplasticité renforcée, et ce tant chez les patients en phase subaiguë que chronique. Une méta-analyse complémentaire publiée dans Frontiers in Neuroscience chiffre l’effet global à 0,56 — modéré en termes statistiques, mais cliniquement significatif pour un patient qui cherche à retrouver l’usage de sa main.
Ce qui rend les BCI particulièrement prometteurs, c’est leur mode de fonctionnement en boucle fermée. Le patient tente mentalement un mouvement. Le dispositif capte le signal cérébral correspondant, le traduit en retour visuel ou en stimulation musculaire directe — et ce couplage précis entre l’intention et la réponse est exactement ce qui force le cerveau à reconstruire ses propres circuits endommagés. Là où la rééducation traditionnelle sollicite le corps, la BCI sollicite simultanément le cerveau qui commande ce corps. C’est cette différence qui change tout.
Les limites existent, et les chercheurs ne les cachent pas. Les effets à long terme restent insuffisamment documentés : les gains peuvent plafonner sans intervention continue, et Liu et al. appellent explicitement à des études multicentriques à grande échelle pour consolider la fiabilité clinique de ces approches. Mais sur un point au moins, le consensus est net : les dispositifs non invasifs utilisés en rééducation — majoritairement basés sur l’EEG — sont sûrs. Aucun effet indésirable majeur n’est rapporté dans les revues systématiques disponibles à ce jour.
Ce que la science dit, en somme : les BCI fonctionnent. Ce qu’elle ne dit pas encore : pour qui, exactement, selon quel protocole, et avec quels effets au-delà de six mois. C’est précisément là que la recherche s’accélère.
Quels sont les principaux obstacles au déploiement clinique des BCI ?
Les obstacles sont techniques, économiques et réglementaires. Sur le plan technique, les blessures cérébrales liées à l’AVC altèrent les caractéristiques dynamiques des signaux EEG, ce qui rend la détection de l’intention motrice moins précise que chez des sujets sains. La variabilité inter-individuelle est forte : les protocoles doivent être personnalisés en fonction de la localisation et de l’étendue de la lésion, de l’âge du patient et de son stade de récupération.
Sur le plan économique, les dispositifs BCI restent coûteux (entre 3 000 et 15 000 euros selon les systèmes), non remboursés dans la plupart des pays, et requièrent une formation spécialisée des équipes soignantes. L’équité d’accès est un enjeu majeur : les patients qui bénéficieront le plus de ces technologies sont souvent ceux qui ont le moins accès aux soins de pointe — sujets âgés, populations défavorisées, résidents en zones rurales sans plateau technique neurologique.
Au-delà de l’AVC : la révolution silencieuse de la neuroplasticité thérapeutique
La rééducation post-AVC n’est que la pointe visible d’un iceberg thérapeutique. Les BCI sont en cours d’évaluation clinique pour la sclérose en plaques, les lésions médullaires, la maladie de Parkinson, les troubles de l’attention (TDAH) et même certaines formes de dépression résistante. Dans tous ces cas, la logique est identique : utiliser la technologie pour potentialiser la capacité du cerveau à se recâbler lui-même.
Une étude publiée par le CNRS souligne que les troubles de l’attention (TDAH) seraient associés à l’intrusion d’ondes du sommeil pendant l’éveil — un résultat qui ouvre la voie à des protocoles BCI de neuromodulation ciblant spécifiquement ces patterns électrophysiologiques. La frontière entre rééducation et augmentation cognitive commence à se brouiller, et avec elle les questions éthiques que la société n’est pas encore prête à trancher.
Euralink et les BCI invasifs : une autre planète
Il est important de distinguer les BCI non invasifs (électrodes de surface, EEG portable) des dispositifs implantés comme Neuralink. Ces derniers offrent une résolution du signal nettement supérieure — permettant des applications comme le contrôle d’un curseur ou d’un bras robotique par la pensée chez des patients tétraplégiques — mais au prix d’une intervention neurochirurgicale et de risques infectieux et mécaniques à long terme non encore pleinement documentés. Les BCI portables pour la rééducation post-AVC relèvent d’une logique clinique radicalement différente : moins spectaculaire, plus sûre, et potentiellement universellement déployable.
La vraie révolution n’est peut-être pas dans le patient qui pilote un drone avec son cerveau, mais dans celui qui, après un AVC, retrouve la capacité d’attraper une tasse de café. La neuroplasticité, enfin mise au service de la médecine réparatrice du quotidien.
Les interfaces cerveau-machine (BCI) sont désormais cliniquement validées pour améliorer la récupération motrice post-AVC, notamment en phase subaiguë. Elles fonctionnent en capturant l’intention motrice du patient et en stimulant les muscles en temps réel, activant la neuroplasticité. Des dispositifs portables permettent désormais la rééducation à domicile (Magnetic NeuroRing). Les obstacles restent techniques (variabilité individuelle), économiques (coût élevé, non remboursé) et d’équité. Les BCI sont également explorés pour le Parkinson, le TDAH et les lésions médullaires. La distinction entre BCI invasifs (Neuralink) et portables est essentielle pour comprendre les enjeux cliniques réels.